Карбонат натрия: свойства, применение, преимущества
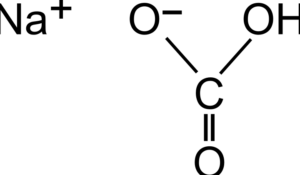
Карбонат натрия (Na2CO3) – это белый кристаллический порошок, который широко используется в промышленности и бытовом хозяйстве. Он содержит два атома натрия, одну молекулу углекислого газа и одну молекулу воды.
Карбонат натрия обладает множеством полезных свойств и применений. В пищевой промышленности он используется как регулятор кислотности, а также как средство для подкрашивания и консервирования продуктов. Он может быть применен для удаления пятен, отбеливания тканей и очистки посуды.
Одним из главных преимуществ карбоната натрия является его способность растворяться в воде и образовывать щелочной раствор. Это позволяет использовать его в производстве стекла, мыла, моющих средств и других химических продуктов.
Карбонат натрия также широко применяется в медицине. Он используется для лечения различных заболеваний, включая расстройства пищеварения, инфекции кожи и глазные проблемы. Кроме того, он может быть использован в качестве антисептика и антимикробного средства.
Производство
Химический способ
Один из основных способов получения карбоната натрия — это химический способ. Он заключается в обработке соли лимоннокислым натрием (Na2C2O4) или карбонатом натрия (Na2CO3) с кислотами. Например, при воздействии уксусной кислоты на карбонат натрия образуется углекислый газ и реакционная смесь, из которой после фильтрации получают гидрокарбонат натрия (NaHCO3). После нагревания гидрокарбонат разлагается, образуя карбонат натрия.
Промышленное производство
Промышленное производство карбоната натрия осуществляется с помощью кальцинированной соды — натриевого карбоната, полученного при нагревании природной соды (Na2CO3 · 10H2O). Кальцинированная сода применяется в качестве основного источника натрия для производства карбоната натрия. Она содержит не менее 98% Na2CO3 и представляет собой белый кристаллический порошок.
Для получения карбоната натрия кальцинированную соду растворяют в воде, а затем добавляют к ней избыток карбоната натрия, чтобы образовался нерастворимый осадок гидрокарбоната натрия (NaHCO3). Полученный осадок отделяют, а оставшуюся жидкость отфильтровывают. Затем полученную жидкость нагревают, пока вся жидкость не испарится, и остается только карбонат натрия.
Применение
Карбонат натрия широко используется в различных отраслях промышленности и имеет множество применений. Он применяется в пищевой промышленности для регулирования кислотности и pH продуктов, таких как соки и напитки. Карбонат натрия также используется в производстве стекла, мыла, моющих средств, а также в качестве отбеливающего и моющего средства для белья.
Благодаря своим свойствам карбонат натрия нашел применение и в косметической промышленности. Он добавляется в состав средств по уходу за кожей, так как помогает поддерживать естественный pH кожи и улучшает ее состояние.
Карбонат натрия также применяется в производстве бумаги, текстиля, керамики и других материалов. Он используется в химической промышленности для получения различных химических соединений, таких как сульфат натрия, тартрат натрия, азид натрия, гексацианоферриат натрия и другие. Также карбонат натрия используется в производстве теста для выпечки, чтобы придать ему нужную консистенцию и улучшить его внешний вид.
Хранение и безопасность
Карбонат натрия должен храниться в сухом и прохладном месте в плотно закрытой таре. Он должен быть защищен от воздействия влаги и кислот. В случае попадания на кожу или в глаза необходимо промыть их большим количеством воды. Работа с карбонатом натрия должна проводиться в соответствии с кстандартной процедурой безопасности.
Обращение с карбонатом натрия должно осуществляться с соблюдением мер предосторожности и правил безопасности. Карбонат натрия является кислотной солью и может вызывать раздражение кожи и слизистых. При работе с ним необходимо использовать защитные средства, такие как перчатки и средства защиты глаз.
Также следует помнить, что карбонат натрия является щелочным веществом и может взаимодействовать с кислотами, образуя газы или творя реакции. При смешивании карбоната натрия с кислотами необходимо быть осторожным и проводить реакцию в хорошо проветриваемом помещении или под вытяжкой.
Промышленный аммиачный способ Сольве
При промышленном аммиачном способе Сольве сначала получают гидрокарбонат натрия, а затем преобразуют его в карбонат натрия. Реакция превращения гидрокарбоната натрия в карбонат натрия происходит при повышенной температуре (около 300°C) и длится определенный срок.
Получение гидрокарбоната натрия
Для получения гидрокарбоната натрия сначала получают раствор аммиака и гидрокарбоната натрия. Затем этот раствор подвергают разложению по следующему методу: к раствору добавляют карбонат натрия и нагревают до 60-70°C. При этой температуре раствор разлагается на гидрокарбонат натрия и аммиак:
- 2NH4Cl + Na2CO3 + 2H2O → 2NH3 + 2NaHCO3 + 2HCl
- 2NH3 + 2NaHCO3 → 2NH4HCO3 + 2NaCl
Полученный гидрокарбонат натрия затем используют для получения карбоната натрия.
Получение карбоната натрия
Для получения карбоната натрия гидрокарбонат натрия подвергают нагреванию при температуре около 300°C. При этой температуре гидрокарбонат натрия разлагается на карбонат натрия, аммиак и воду:
2NaHCO3 → Na2CO3 + CO2 + H2O
Полученный карбонат натрия может быть использован в различных отраслях, таких как химическая промышленность, кулинария, пожаротушение и другие.
Применение и преимущества
Карбонат натрия используется в производстве стекла, моющих средств, моющих порошков, моющих средств для посуды, стиральных порошков и других химических продуктов. Также он применяется в кулинарии, например, для приготовления лимоннокислого глютамата натрия.
Одним из преимуществ промышленного аммиачного способа Сольве является безопасность, так как аммиак не является опасным веществом при правильном использовании. Также этот способ получения карбоната натрия более экономичен, чем другие методы.
Важно отметить, что при хранении карбоната натрия необходимо соблюдать определенные меры предосторожности, так как он может реагировать с кислотами, например, соляной кислотой или хлористокислым раствором, и выделять углекислый газ.
Нахождение в природе
Карбонат натрия также может быть получен из раствора, в котором содержится соль карбоната и гидроксид натрия. Последний реагирует с кислотой и образует карбонат натрия. Карбонат натрия может быть получен также путем нагрева бикарбоната соды или разложения соли с кислотой, например, уксусной или сольве квасцовой. Иногда карбонат натрия получают путем реакции саркозината натрия или оксалата натрия с аммиаком.
В промышленности карбонат натрия широко используется для производства стекла, мыла, моющих средств, бумаги, текстиля и других продуктов. Он также применяется в кулинарии в качестве пищевой добавки и в производстве различных продуктов питания, таких как кондитерские изделия, мороженое и газированные напитки.
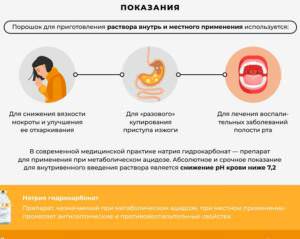
Карбонат натрия может быть использован в медицине для лечения некоторых болезней и состояний, таких как изжога и снижение кислотности желудка. Он также иногда используется в качестве отбеливателя и дезинфицирующего средства.
Карбонат натрия находит применение в разложении солей и получении ряда золотых соединений, таких как соль салицилат, соль хлористокислый, соль хромат, соль сульфата, соль селенат, соль молибдат и титанат. Он также используется в производстве промышленных осадков и пыли.
Срок хранения карбоната натрия ограничен, так как он разлагается при воздействии влаги и углекислого газа. Натрий карбонат также растворим в аммиачном растворе.
В транспорте
| Область применения | Описание |
|---|---|
| Производство стекла | Карбонат натрия является важным сырьем для производства стекла. Он используется для понижения температуры плавления и улучшения свойств стекла. |
| Производство мыла | Карбонат натрия используется в производстве мыла, где он служит в качестве щелочного вещества для реакции с жирами и маслами. |
| Очистка воды | Карбонат натрия используется для увеличения pH растворов воды и уменьшения кислотности. Это помогает в удалении загрязнений и обеспечении безопасности воды для питья. |
| Производство перекиси водорода | Карбонат натрия может быть использован для производства перекиси водорода путем реакции с кислотами, такими как серная кислота или оксалат. |
| Хранение продуктов | Карбонат натрия используется для увеличения срока годности продуктов, таких как соки и газированные напитки. Он помогает сохранять свежесть и предотвращает разложение продуктов. |
Химические свойства
Карбонат натрия (Na2CO3) обладает рядом химических свойств, которые определяют его применение в различных областях.
Растворимость и реакция с кислотами
Карбонат натрия хорошо растворяется в воде, образуя раствор, который имеет слабо щелочную реакцию. При взаимодействии с кислотами происходит нейтрализационная реакция, в результате которой образуются соли и выделяется углекислый газ:
- С раствором соляной кислоты (HCl) образуется хлорид натрия (NaCl), вода (H2O) и углекислый газ (CO2):
- С раствором уксусной кислоты (CH3COOH) образуется ацетат натрия (CH3COONa), вода (H2O) и углекислый газ (CO2):
- С раствором солянокислого калия (H2SeO3) образуется селенистокислый натрий (Na2SeO3), вода (H2O) и углекислый газ (CO2):
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
Na2CO3 + 2CH3COOH → 2CH3COONa + H2O + CO2
Na2CO3 + H2SeO3 → Na2SeO3 + H2O + CO2
Реакция с кислородсодержащими соединениями
Карбонат натрия реагирует с кислородсодержащими соединениями, такими как перманганат калия (KMnO4) и перекись водорода (H2O2), образуя окисленные продукты.
Реакция с цирконатом аммония
При взаимодействии с цирконатом аммония (NH4)2ZrO(CO3)2 методом сольве-гидротермального синтеза образуется комплексный цирконат натрия и аммония.
Получение и выделение
Карбонат натрия получают путем обработки цирконатом натрия при температуре около 1000 °C:
- Цирконат натрия (Na2ZrO3) подвергают термическому разложению:
- Полученный оксид натрия (Na2O) реагирует с углекислым газом (CO2), образуя карбонат натрия (Na2CO3):
Na2ZrO3 → Na2O + ZrO2
Na2O + CO2 → Na2CO3
Выделение карбоната натрия из раствора осуществляется путем его кристаллизации или дополнительной обработки раствора специальными методами.
Способы хранения
Карбонат натрия хранят в герметично закрытой упаковке в сухом месте при температуре не выше 25 °C. Срок годности составляет 3 года.
Безопасность
Карбонат натрия является сравнительно безопасным веществом, однако при контакте с кожей или слизистыми оболочками может вызвать раздражение. При попадании в глаза следует промыть их водой и обратиться к врачу. Для работы с карбонатом натрия рекомендуется использовать средства индивидуальной защиты.
Применение
Карбонат натрия широко применяется в разных областях:
- В пищевой промышленности используется в качестве пищевой добавки (E500) для регулирования кислотности и улучшения текстуры пищевых продуктов, таких как хлеб, конфеты, печенье и другие.
- В производстве стекла и керамики применяется для улучшения прозрачности и прочности изделий.
- В химической промышленности используется в качестве сырья для получения других химических соединений, таких как карбонаты калия и лития, этоксид натрия и др.
- В медицине используется в качестве антацидного препарата для снижения кислотности желудочного сока и уменьшения изжоги.
- В минеральной промышленности применяется для выделения и очистки минералов из руд.
- В пожаротушении используется как компонент пеногенераторов для создания пены, которая эффективно гасит пожары.
Способ Леблана
В промышленном производстве карбоната натрия способ Леблана был одним из основных до начала 20 века. Однако с развитием процесса Солве и Хоу, его использование стало не таким распространенным.
Способ Леблана также нашел применение в кулинарии. Например, при приготовлении хлеба, для улучшения качества теста, добавляют натрия карбоната. Также в производстве пищевых продуктов используют перкарбонат натрия, который при взаимодействии с водой высвобождает активный кислород, обладающий отбеливающими свойствами.
Способ Леблана имеет свои преимущества и недостатки. Он позволяет получить высококачественный карбонат натрия сравнительно низкой стоимостью, но требует использования определенных химических реагентов, таких как аммиак и хлорид натрия.
В медицине карбонат натрия используется для регулирования кислотности в организме. Он также применяется в химическом анализе для определения содержания хлора и йодатов.
При хранении карбонат натрия следует избегать контакта с веществами, такими как селенистый кислота, йодат натрия и хромат натрия, так как это может привести к образованию опасных соединений. Также не рекомендуется хранить карбонат натрия в близком контакте с продуктами, содержащими глютамат натрия, пропионат натрия, хлористокислый натрий и другие.
Преимущества способа Леблана:
- Относительно низкая стоимость производства карбоната натрия;
- Высокое качество получаемого продукта;
- Возможность использования в различных отраслях промышленности и кулинарии.
Недостатки способа Леблана:
- Необходимость использования определенных химических реагентов;
- Возможность образования опасных соединений при неправильном хранении;
- Использование более современных и эффективных методов производства карбоната натрия.
Способ Хоу
Способ Хоу основан на разложении соли, которая называется «сода». Сода содержит два основных компонента: натрий (Na) и карбонат (CO3). Когда сода разлагается, образуется карбонат натрия и углекислый газ (CO2).
Разложение соды происходит при высокой температуре в печи. Для этого используются различные вещества, например, серная кислота, селенистый азид, гексагидроксохромат натрия и другие.
Способ Хоу также используется в пищевой промышленности для получения карбоната натрия из растительных продуктов, таких как золы и соки. Например, при производстве лимоннокислого натрия из лимонов используется раствор саркозината натрия.
Способ Хоу имеет ряд преимуществ. Он позволяет получить высокопрочный и стабильный продукт, который можно использовать в различных областях, таких как производство стекла, керамики, моющих средств и многих других. Карбонат натрия также используется в кулинарии, в процессе пожаротушения и хранения продуктов.
Однако, при использовании карбоната натрия необходимо соблюдать меры безопасности, так как он может быть опасен при попадании на кожу или в глаза. Также стоит учитывать, что карбонат натрия разлагается в воде, образуя щелочную соль, поэтому его не рекомендуется использовать с кислотными продуктами.
В химической промышленности
Карбонат натрия имеет широкое применение в химической промышленности благодаря своим уникальным свойствам. Он широко используется для получения различных химических соединений и средств бытовой химии.
В производстве кожи карбонат натрия используется для образования реакции между карбонатом натрия и кислотами, такими как гидроокись натрия и сульфат натрия. Полученный раствор применяется для обработки кожи, повышая ее прочность и устойчивость к воздействию воды.
В пищевой промышленности карбонат натрия применяется для получения различных пищевых добавок. Например, с его помощью получают сольве, а также соду. Карбонат натрия добавляют в воду или сок при приготовлении напитков для регулирования pH и придания особого вкуса.
В химической промышленности карбонат натрия используется в процессе получения многих химических соединений. Например, для получения глютамата натрия используется реакция между карбонатом натрия и аммиаком при высокой температуре. Также карбонат натрия применяется для получения карбоната цирконата, ванадиевокислого натрия и других соединений.
Карбонат натрия также находит применение в производстве стекла. Он используется для повышения термической стабильности стекла и улучшения его оптических свойств.
Также карбонат натрия применяется в кулинарии. Он используется для приготовления различных блюд и выпечки. Например, карбонат натрия добавляют в тесто для придания воздушности и объема выпечке.
В химической промышленности карбонат натрия также используется для получения различных минералов из золы угльных топлив. Например, карбонат натрия используется для извлечения карбоната натрия, гексацианоферриата натрия и других соединений из золы.
Таким образом, карбонат натрия играет важную роль в химической промышленности, обладая уникальными свойствами и широким спектром применения.
В кулинарии
Карбонат натрия (Na2CO3) находит широкое применение в кулинарии благодаря своим полезным свойствам. Белая кристаллическая соль, также известная как пищевая сода, обладает рядом химических и физических свойств, которые делают ее неотъемлемой частью многих рецептов и приготовлений.
Карбонат натрия используется в кулинарии для регулирования кислотности продуктов. Он является слабой щелочью и может нейтрализовать кислоты, повышая pH продукта. Благодаря этому свойству, карбонат натрия часто используется при выпечке, чтобы придать тесту более пышную и мягкую текстуру.
Он также применяется в процессе образования осадка при приготовлении некоторых блюд. При добавлении карбоната натрия в раствор кислоты происходит образование гидроксида натрия (NaOH) и углекислого газа (CO2). Это приводит к образованию пузырьков и повышает объем теста или тесто.
Карбонат натрия также широко используется в кулинарии для обработки продуктов. Он может использоваться для удаления запахов и нежелательных вкусов, а также для консервации пищевых продуктов. Например, он может быть добавлен в рассол для консервации овощей или воды для варки мяса.
Карбонат натрия также может быть использован как стабилизатор для взбитых сливок или яичных белков. Он помогает сохранять структуру и плотность этих продуктов, предотвращая разложение и истекание.
Карбонат натрия также может быть использован для приготовления различных соусов и дрессингов. Например, он может быть добавлен в соусы для придания им кремовой текстуры и регулирования кислотности.
В кулинарии также применяются другие соединения натрия, такие как бикарбонат натрия (NaHCO3) и гидроксид натрия (NaOH). Бикарбонат натрия обладает свойством выпускать углекислый газ при нагреве, что делает его идеальным для приготовления пышек и теста. Гидроксид натрия используется в кулинарии для обработки овощей и фруктов, а также для регулирования pH растворов.
Хранение
Продукт должен храниться в сухом и прохладном месте, в закрытой таре, чтобы избежать попадания влаги и воздуха. Карбонат натрия не должен храниться вместе с кислотами, поскольку они могут вызвать химическую реакцию и повредить продукт.
Также необходимо избегать контакта карбоната натрия с гидроксидом натрия, аммиаком и аммиачными солями, так как это может привести к образованию опасного газа — аммиака. Карбонат натрия несовместим с некоторыми другими химическими веществами, такими как перкарбонат натрия, пероксид водорода и др.Срок годности карбоната натрия зависит от условий хранения и может составлять несколько лет. Однако, с течением времени продукт может подвергаться окислению и потере своих свойств. При хранении карбоната натрия следует регулярно проверять его состояние и, при необходимости, заменять его новым.
Читайте далее: