Гидрокарбонат натрия: свойства, применение, польза и вред
Гидрокарбонат натрия, также известный как сода или бикарбонат натрия (NaHCO3), является химическим соединением, которое обладает широким спектром свойств и применений. Его идеальное свойство — термическое разложение, которое происходит при низкой температуре, протекает плавно и без взрыва. Это делает его безопасным в использовании в различных областях, включая промышленность, медицину и кулинарию.
В кулинарии гидрокарбонат натрия используется, например, для приготовления теста. Зачем правильно его использовать? Когда соду добавляют в тесто вместе с уксусом или кефиром, начинается реакция, в результате которой образуется газ (CO2↑+ H2O) и тесто становится пышным и воздушным. Это свойство соды также позволяет использовать ее в качестве порошка для выпечки.
В промышленности гидрокарбонат натрия также находит широкое применение. Например, его используют для производства стекла, моющих средств, медикаментов и других химических продуктов. Благодаря своим свойствам гидрокарбонат натрия может быть использован в качестве средства пожаротушения. При контакте со сгорающими веществами он реагирует с ними, выделяя CO2 газ, который гасит огонь.
Однако, несмотря на все его полезные свойства, гидрокарбонат натрия также имеет свои противопоказания и ограничения. Например, при попадании в глаза или на кожу может вызвать раздражение и ожоги. Поэтому необходимо соблюдать меры предосторожности при работе с содой. Кроме того, гидрокарбонат натрия не рекомендуется употреблять в больших количествах, так как это может привести к возникновению проблем со здоровьем, например, нарушению рН крови.
Применение
Гидрокарбонат натрия (NaHCO3), также известный как пищевая сода или сода, имеет широкий спектр применения в различных областях, благодаря своим уникальным свойствам.
В кулинарии
Сода является важным ингредиентом при выпечке. Она используется в качестве разрыхлителя, добавляя пористость и легкость тесту. При взаимодействии с кислотой, такой как уксус (CH3COOH), гидрокарбонат натрия начинает распадаться на газ (CO2) и воду (H2O), что приводит к образованию пузырьков и вздутию теста. Поэтому сода и уксус вместе являются идеальной комбинацией для приготовления пышных блинов, оладий и других выпечек.
Примечание: При использовании соды в кулинарии важно правильно дозировать ее количество, чтобы не переборщить и не испортить вкус блюда.
В хозяйственных целях
Сода также находит применение в быту. Она может использоваться для удаления неприятных запахов, чистки поверхностей и посуды, а также для устранения пятен и разных загрязнений. Сода с Ch3COONa (уксусом) образует газ CO2, который можно использовать для пожаротушения. Поэтому сода часто используется в качестве безопасного агента по гасению различных видов пожаров.
В медицине
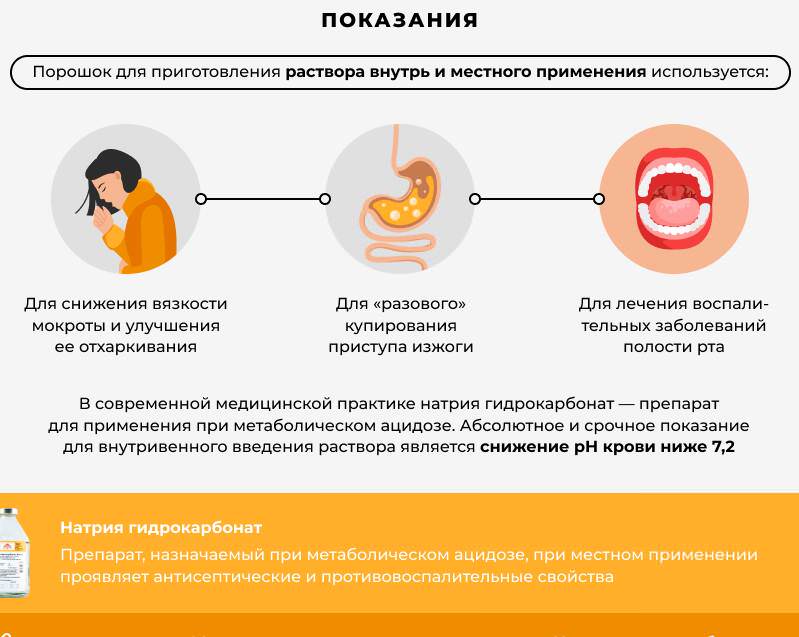
Гидрокарбонат натрия также имеет свои применения в медицине. Например, он может использоваться для облегчения симптомов изжоги и избавления от избытка желудочной кислоты. Сода может также помочь в устранении зубного налета и освежении дыхания.
В промышленности
В промышленности гидрокарбонат натрия находит применение в различных процессах. Например, он используется в производстве стекла, мыла, красителей и многих других химических веществ. Также сода используется для очистки воды и удаления загрязнений.
Все это делает гидрокарбонат натрия полезным и востребованным веществом в разных сферах жизни, однако необходимо помнить о правилах безопасности при его использовании.
Производство
Идеальный способ производства гидрокарбоната натрия – это термическое разложение натрийкарбоната (Na2CO3) при температуре около 50-70°C:
Реакция производства гидрокарбоната натрия:
2Na2CO3 + H2O + CO2 → 2NaHCO3 + CO2↑
Процесс начинается с представления натрийкарбоната (Na2CO3) в виде порошка. Затем порошок нагревается и происходит реакция, в результате которой натрийкарбонат распадается на гидрокарбонат натрия и углекислый газ.
Гидрокарбонат натрия имеет свойства, которые делают его полезным в различных областях. Например, его можно использовать в медицине для гасения кислотами, а также в промышленности для различных химических процессов. В кулинарии гидрокарбонат натрия добавляют в тесто, чтобы оно правильно поднялось. Он также используется в пожаротушении для гашения пожаров с помощью уксуса и кефира.
Польза гидрокарбоната натрия состоит в его способности гасить кислоты и предотвращать разложение пищевых продуктов. Он также может быть использован для хранения угольной кислоты и теста, чтобы предотвратить их распад. В качестве примечания, гидрокарбонат натрия также известен как пищевая сода или пищевой газ.
Таким образом, гидрокарбонат натрия имеет широкое применение в различных отраслях и обладает ценными свойствами. Его производство осуществляется путем термического разложения натрийкарбоната, а полученный продукт может быть использован в медицине, промышленности и кулинарии.
Безопасность
Химические свойства и реакция с другими веществами
Гидрокарбонат натрия при нагревании распадается на соль, углекислый газ и воду. Термическое разложение протекает при температуре около 50°С. Например, при смешивании с уксусом (CH3COOH) образуется углекислый газ (CO2↑+ H2O) и ацетат натрия (CH3COONA). Гидрокарбонат натрия также может реагировать с кислотами, например, с уксусной кислотой, образуя соль и выделяя углекислый газ.
Применение в кулинарии
В кулинарии гидрокарбонат натрия используется для приготовления различных блюд. Он используется, например, для гашения теста, чтобы придать ему объем и пушистость. Гидрокарбонат натрия активируется в контакте с кислотой и начинает выделять углекислый газ, что способствует подъему теста. Однако следует помнить, что неправильное использование соды или неправильное соотношение с другими ингредиентами может негативно сказаться на вкусе и текстуре блюда.
Примечания по безопасному использованию
При использовании гидрокарбоната натрия следует соблюдать определенные меры предосторожности:
- Хранить соду в герметичной упаковке, вдали от влаги и кислот;
- Не допускать попадания соды в глаза или на кожу;
- Не употреблять соду внутрь в больших количествах, так как это может вызвать негативные последствия для здоровья;
- Использовать соду только по назначению и в соответствии с рецептами.
Гидрокарбонат натрия является важным компонентом в различных сферах, включая производство, химическую промышленность, кулинарию и медицину. Однако, несмотря на свои полезные свойства, сода может быть опасной, если использована неправильно или в больших количествах. Поэтому необходимо соблюдать меры безопасности при работе с ней и использовать ее с умом.
Зачем гасить соду уксусом
Сода и уксус (CH3COOH) реагируют между собой, образуя углекислый газ (CO2↑+), воду (H2O) и ацетат натрия (CH3COONA). Эта реакция является термической, то есть происходит при повышенной температуре.
Гашение соды уксусом имеет несколько полезных свойств. Во-первых, при гашении сода начинает распадаться на угольную кислоту и натриевую соль, что позволяет уменьшить ее концентрацию и сделать ее более безопасной для использования. Во-вторых, образующийся углекислый газ может использоваться в качестве средства пожаротушения или для создания идеального порошка для выпечки. Также гашение соды уксусом может быть полезно в хозяйстве, например, для удаления неприятных запахов или очищения поверхностей.
При гашении соды уксусом следует соблюдать определенные меры безопасности. Реакция может протекать достаточно быстро, поэтому необходимо быть осторожным и избегать контакта с газом и жидкостью. Рекомендуется проводить гашение соды уксусом в хорошо проветриваемом помещении и надевать средства индивидуальной защиты.
Таким образом, гашение соды уксусом представляет собой химическую реакцию, при которой образуется углекислый газ. Этот процесс находит свое применение в различных сферах, включая промышленность, кулинарию и медицину. Гашение соды уксусом также имеет полезные свойства, однако требует соблюдения мер безопасности при выполнении.
| Гидрокарбонат натрия (NaHCO3) | Уксус (CH3COOH) | Углекислый газ (CO2) | Ацетат натрия (CH3COONA) |
|---|---|---|---|
| Сода | Уксус | Газ+вода | Соль уксуса |
Примечания: гашение соды уксусом также известно как «распадание соды», «разложение соды» или «газование соды».
Химические свойства
Гидрокарбонат натрия (NaHCO3), также известный как сода, представляет собой соль, которая распадается при термическом разложении на углекислый газ (CO2) и воду (H2O). Эта реакция протекает при температуре около 50-60 °C.
Сода также может реагировать с различными кислотами, например, с уксусной кислотой (CH3COOH), образуя соль – ацетат натрия (CH3COONa). При этом образуется углекислый газ (CO2↑) и вода (H2O). Именно эту реакцию можно использовать при гашении пожаров, так как углекислый газ является негорючим газом и благоприятно влияет на процесс тушения.
Сода находит широкое применение в различных областях. В кулинарии ее добавляют в тесто для получения пышного и мягкого изделия. Также сода используется для приготовления различных газированных напитков, в том числе кефира.
В промышленности гидрокарбонат натрия используется в производстве стекла, моющих средств, мороженого и других продуктов. В медицине сода применяется для лечения некоторых заболеваний и как антацидное средство.
Сода обладает хорошей сроком годности, но требует особого хранения в сухом месте и в герметичной таре. Не рекомендуется хранить соду вблизи продуктов, которые могут поглощать запахи.
| Примечания: |
|---|
| Сода можно гасить уксусом, но необходимо быть осторожным при проведении данной реакции, так как она может быть опасной. |
Термическое разложение
Сода (гидрокарбонат натрия) обладает свойством термического разложения при нагревании. При температуре около 50°C сода начинает распадаться на два продукта: углекислый газ (CO2) и воду (H2O). Реакция разложения соды представляет собой следующее уравнение:
2NaHCO3 -> Na2CO3 + CO2↑ + H2O
Говоря простым языком, при нагревании сода распадается на натриевый карбонат, углекислый газ и воду.
Применение в кулинарии
Термическое разложение соды на газ и воду делает ее идеальным ингредиентом для выпечки. Добавленная в тесто, сода помогает тесту подняться и стать более воздушным. Также, сода используется в качестве ингредиента для гашения уксуса. Например, когда в рецепте требуется смешать соду и уксус, происходит реакция между ними, при которой выделяется углекислый газ и вода.
Применение в промышленности и медицине
Гидрокарбонат натрия также находит применение в промышленности, например, в производстве стекла и моющих средств. В медицине сода используется для нейтрализации кислотности желудочного сока, а также в качестве средства для пожаротушения при горении угольной кислоты (H2CO3).
Правильное хранение и безопасность
Сода натрия является безопасным веществом, однако при хранении следует соблюдать определенные меры предосторожности. Сода должна храниться в герметично закрытой упаковке, в сухом месте, вдали от прямых солнечных лучей. Также, не рекомендуется хранить соду вместе с кислотами, так как они могут вызвать реакцию разложения соды.
Примечания:
- CO2 — углекислый газ
- CH3COOH — уксусная кислота
- CH3COONa — ацетат натрия
- NaHCO3 — гидрокарбонат натрия (сода)
- Na2CO3 — натриевый карбонат (соль)
Пожаротушение
Гидрокарбонат натрия, или сода, широко используется в качестве пожаротушителя благодаря своим уникальным свойствам.
При контакте с огнем гидрокарбонат натрия распадается на углекислый газ (CO2) и воду (H2O). Реакция протекает при температуре выше 50 градусов Цельсия. Гидрокарбонат натрия начинает распадаться на углекислый газ и воду при нагревании, что позволяет использовать его для тушения пожаров.
При пожаротушении с использованием гидрокарбоната натрия, также известного как сода, происходит следующая реакция:
- NaHCO3 (гидрокарбонат натрия) + CH3COOH (уксусная кислота) → CH3COONa (ацетат натрия) + CO2↑ + H2O
Уксусная кислота, которая является основным компонентом уксуса, реагирует с гидрокарбонатом натрия, образуя ацетат натрия, углекислый газ и воду. Газ CO2↑, выделяющийся при этой реакции, давит на огонь и гасит его.
Сода также широко используется в промышленности и в быту. Например, в кулинарии ее добавляют в тесто для придания объема и воздушности выпечке. В медицине гидрокарбонат натрия применяется в качестве лекарственного препарата для нейтрализации кислотности в желудке. Кроме того, сода используется для тушения термического горения, такого как горение масла или жира.
Сода хранится в сухом месте, так как при попадании влаги она может подвергнуться разложению. Также важно соблюдать меры безопасности при использовании гидрокарбоната натрия в качестве пожаротушителя, так как при его реакции с кислотой может выделяться углекислый газ, который представляет опасность для дыхания.
В идеальном случае, для пожаротушения рекомендуется использовать порошок гидрокарбоната натрия, который содержит соду, а также другие химические соединения, улучшающие его свойства и эффективность.
Медицина
Гидрокарбонат натрия, или сода, имеет широкий спектр применения в медицине. Этот химический соединение часто используется для лечения различных заболеваний и состояний.
Свойства и применение
Гидрокарбонат натрия обладает антикислотными свойствами и может быть использован в качестве антацидного препарата при избыточной кислотности желудочного сока. Он также может использоваться для облегчения симптомов изжоги и газообразования.
В кулинарии гидрокарбонат натрия употребляется для гашения уксусом и добавления в различные блюда. Например, он может использоваться для приготовления теста, чтобы оно стало более пышным.
Производство и хранение
Гидрокарбонат натрия может быть произведен с помощью реакции между натрием и угольной кислотой. При этом образуется углекислый газ и вода. Полученный гидрокарбонат натрия представляет собой белый порошок, который имеет длительный срок хранения при правильном хранении.
Для безопасности при использовании гидрокарбоната натрия необходимо соблюдать определенные меры предосторожности. Не рекомендуется превышать рекомендуемую дозу и использовать его без консультации с врачом.
Важно также помнить, что гидрокарбонат натрия может вызывать аллергические реакции у некоторых людей. Поэтому перед использованием следует провести тест на аллергию.
Вывод: гидрокарбонат натрия имеет широкий спектр применения в медицине. Он может быть использован для лечения различных заболеваний и состояний, а также в кулинарии и промышленности.
Кулинария
Гидрокарбонат натрия, также известный как сода, имеет широкое применение в кулинарии. Это безопасное вещество, которое может быть использовано для различных целей.
Одним из главных свойств соды является ее способность взаимодействовать с кислотами. Например, сода может реагировать с уксусом (CH3COOH) и образовывать уксуснокислый натрий (CH3COONa) и углекислый газ (CO2↑+H2O). Эта реакция может быть использована в кулинарии для газирования теста или гашения кефира. Для гашения соды обычно используют уксус, так как он безопасен для пищевого применения и не имеет неприятного запаха.
Сода также представляет собой идеальный ингредиент для хранения порошка. Она не только предотвращает застывание порошка, но и увеличивает его срок годности. Добавление соды в порошок также может предотвратить его термическое разложение при высоких температурах.
В кулинарии сода может быть использована для приготовления различных блюд. Например, она может быть добавлена в тесто для приготовления пышных и мягких изделий. Также сода может быть использована для приготовления пожаротушащих средств. Реакция соды с уксусом приводит к выделению углекислого газа, который может использоваться для гашения маленьких пожаров.
В промышленности сода используется для производства различных продуктов, включая соль, уксус и углекислый газ. Кроме того, она находит применение в медицине для лечения некоторых заболеваний и облегчения некоторых симптомов.
| Свойства соды | Применение | Польза | Вред |
|---|---|---|---|
| Распадается при нагревании | Газирование теста | Улучшение структуры блюд | Избегать перегрева |
| Реакция с кислотами | Гашение кефира, пожаротушение | Безопасность использования | Избегать контакта с кожей и глазами |
| Увеличивает срок годности порошка | Хранение порошка | Предотвращение застывания | Использовать в умеренных количествах |
| Применяется в промышленности | Производство соли, уксуса, углекислого газа | Разнообразие продуктов | Не использовать в больших количествах |
Примечания: CH3COOH — уксусная кислота, CH3COONa — ацетат натрия
NaHCO3 + CH3COOH → CH3COONa + CO2↑+ H2O
Реакция между гидрокарбонатом натрия (NaHCO3) и уксусной кислотой (CH3COOH) приводит к образованию ацетата натрия (CH3COONa), углекислого газа (CO2↑) и воды (H2O). Эта химическая реакция широко используется в различных областях, включая кулинарию, медицину и промышленность.
В кулинарии гидрокарбонат натрия используется для приготовления различных изделий, таких как тесто. При взаимодействии с уксусом, сода представляет собой идеальный порошок для гашения, который активно используется хозяйками. Реакция между содой и уксусом приводит к быстрому образованию углекислого газа и воды, что позволяет тесту хорошо подниматься и стать воздушным.
В медицине гидрокарбонат натрия также находит свое применение. Например, в качестве антацидного средства для снижения кислотности желудочного сока. Сода может быть добавлена в напитки, такие как кефир, для нейтрализации кислотности и смягчения их вкуса.
В промышленности гидрокарбонат натрия используется в производстве различных продуктов. Например, его применяют для очистки и дезинфекции поверхностей, а также в процессе производства стекла и мыла. Кроме того, сода может использоваться для пожаротушения, так как при нагревании она разлагается на углекислый газ и воду, что помогает гасить огонь.
Необходимо отметить, что реакция между гидрокарбонатом натрия и уксусной кислотой является термической реакцией, то есть протекает при нагревании. При этом происходит разложение соды с образованием ацетата натрия, углекислого газа и воды. Реакция не является опасной при правильном использовании и соблюдении мер безопасности.
| Свойства | Применение |
|---|---|
|
— Гидрокарбонат натрия представляет собой белый кристаллический порошок с щелочной реакцией. — Растворяется в воде и обладает слабым щелочным вкусом. — Разлагается при нагревании выше 50 °C, освобождая углекислый газ. — Имеет срок хранения, поэтому необходимо хранить в сухом месте. |
— Используется в кулинарии для приготовления выпечки и теста. — Применяется в медицине как антацидное средство. — Используется в промышленности для производства стекла, мыла и других продуктов. — Применяется для пожаротушения. |
В заключение можно сказать, что гидрокарбонат натрия (NaHCO3) и уксусная кислота (CH3COOH) образуют ацетат натрия (CH3COONa), углекислый газ (CO2↑) и воду (H2O) при их взаимодействии. Эта реакция имеет широкое применение в кулинарии, медицине и промышленности. При правильном использовании и соблюдении мер безопасности, гидрокарбонат натрия может быть полезным и безопасным веществом.
См также
Гидрокарбонат натрия, или сода, имеет широкий спектр применения в различных сферах жизни. В данном разделе рассмотрим несколько интересных свойств и применений этого вещества.
Медицина
Сода, взаимодействуя с уксусом, представляет собой эффективное средство для нейтрализации желудочной кислоты. Например, если у вас возникло изжога, можно растворить небольшое количество соды в воде и выпить этот раствор. Кроме того, сода помогает смягчить симптомы некоторых заболеваний, таких как киста на почке или инфекция мочевыводящих путей.
Кулинария
Сода используется в приготовлении различных блюд. Например, она может быть добавлена в тесто для выпечки, чтобы оно лучше поднялось. Также сода позволяет сохранить свежесть овощей, добавленных в воду для их варки. Иногда соду можно использовать в качестве заменителя уксуса при приготовлении соусов или маринадов.
| Применение | Польза | Вред |
|---|---|---|
| Пожаротушение | Сода может использоваться для гашения пожара, так как при нагревании она распадается на газ и воду, которые гасят огонь. | Необходимо соблюдать меры безопасности при использовании соды для тушения пожара и следовать инструкциям. |
| Производство | Сода используется в промышленности для производства стекла, мыла, бумаги и других продуктов. | При обращении с содой в промышленных условиях необходимо соблюдать правила безопасности и использовать соответствующие средства защиты. |
Кроме того, сода имеет ряд химических свойств, которые проявляются при взаимодействии с различными веществами. Например, сода реагирует с кислотами, образуя соль, воду и углекислый газ (CO2↑+). Эта реакция может протекать даже при обычных условиях, например, при смешивании соды и уксуса. Также сода начинает распадаться при нагревании до температуры около 50 градусов Цельсия, выделяя углекислый газ и воду.
Примечания
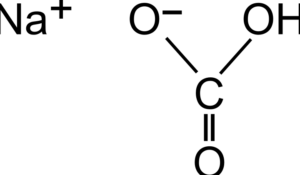
Сода (NaHCO3) также известна как бикарбонат натрия или гидрокарбонат натрия. В химии она обозначается как NaHCO3.
Сода является идеальным средством для гашения угольной кислотой (H2CO3). При этом образуется соль (CH3COONa) и вода.
Сода хорошо сочетается с уксусом (CH3COOH), образуя соль (CH3COONa) и выделяя углекислый газ (CO2↑+).
Сода и уксус являются безопасными и широко используемыми продуктами в быту, однако необходимо соблюдать правила безопасности при их использовании.
Реакция с кислотами
Когда гидрокарбонат натрия взаимодействует с уксусной кислотой, происходит реакция, в результате которой образуется углекислый газ (CO2) и ацетат натрия (CH3COONa). Реакция протекает следующим образом:
CH3COOH + NaHCO3 → CH3COONa + H2O + CO2↑
Углекислый газ, который образуется в результате реакции, может использоваться для различных целей. Например, в кулинарии сода используется как разрыхлитель для теста. При взаимодействии с уксусом сода начинает распадаться, выделяя углекислый газ, который захватывает воздушные пузырьки в тесте и делает его более пышным и легким.
Реакция гидрокарбоната натрия с кислотами может быть также использована для пожаротушения. При взаимодействии с кислотой гидрокарбонат натрия гасит огонь, выделяя углекислый газ и воду. Углекислый газ, являющийся инертным газом, подавляет горение и помогает предотвратить распространение огня.
Помимо кулинарии и пожаротушения, гидрокарбонат натрия находит применение в различных областях, таких как медицина, промышленность и производство. В медицине он может использоваться в качестве антацидного средства для уменьшения избыточной кислотности в желудке. В промышленности гидрокарбонат натрия используется для производства стекла, моющих средств и других продуктов. В производстве он может служить в качестве регулятора pH или добавки для регулирования процессов химической реакции.
Свойства и безопасность
Гидрокарбонат натрия представляет собой белый порошок, растворимый в воде. Он имеет щелочные свойства и может вызывать раздражение кожи и слизистых оболочек, поэтому при работе с ним необходимо соблюдать меры безопасности, такие как использование защитных перчаток и очков.
Хранить гидрокарбонат натрия следует в сухом месте при комнатной температуре. При нагревании он может разлагаться с выделением углекислого газа и натриевой соли угольной кислоты.
Примечания
Гидрокарбонат натрия (NaHCO3) иногда называют также идеальным порошком для хозяек, так как он обладает множеством полезных свойств и может использоваться в различных сферах жизни.
Хранение
Сода подвержена разложению при взаимодействии с кислотами. Поэтому при хранении ее необходимо защищать от воздействия кислотных паров. Например, соду не рекомендуется хранить вместе с уксусом, так как уксус является кислотой, и при контакте с содой может произойти реакция:
CH3COOH + NaHCO3 → CH3COONa + CO2↑ + H2O
В результате такой реакции образуется газ (CO2) и вода (H2O), а также ацетат натрия (CH3COONa). Поэтому соду не следует хранить вместе с уксусом.
Также сода может распадаться при повышенной температуре. Поэтому ее не рекомендуется хранить вблизи источников тепла. Распадаясь, сода выделяет углекислый газ (CO2), который может привести к повышенному давлению внутри упаковки и вызвать ее взрыв.
При хранении соды следует обратить внимание на безопасность. Не следует хранить соду в доступе для детей и животных. Также не рекомендуется хранить соду в металлических или алюминиевых контейнерах, так как она может реагировать с металлом и приводить к образованию токсичных соединений.
Идеальным способом хранения соды является плотная упаковка в пластиковые или стеклянные контейнеры с герметической крышкой, которые защитят продукт от влаги и воздействия кислот. Также рекомендуется хранить соду в прохладном и сухом месте при температуре не выше 25 °C.
Важно помнить, что сода имеет ограниченный срок годности. Поэтому перед использованием следует проверить ее на наличие срока годности и не использовать просроченный продукт.
Примечания:
- Соду можно использовать для гашения пожаров, особенно угольных, так как она выделяет углекислый газ, который гасит пламя.
- Сода также находит применение в промышленности, например, при производстве стекла, моющих средств и других химических продуктов.
- Сода может использоваться для пожаротушения в кулинарии. Например, если во время приготовления теста начинает протекать реакция соды с уксусом, то можно добавить немного соды, чтобы остановить реакцию.
Примечания
- Гидрокарбонат натрия (NaHCO3) также известен как сода, пищевая сода или бикарбонат натрия.
- В химии гидрокарбонат натрия используется в качестве промежуточного продукта при производстве уксусной кислоты (CH3COOH).
- Сода широко применяется в кулинарии, например, для гашения соды уксусом (CH3COOH + NaHCO3 → CH3COONa + H2O + CO2↑+).
- Свойства гидрокарбоната натрия включают термическое разложение при высокой температуре и способность реагировать с кислотами, представляя соль и выделяя углекислый газ (CO2).
- В медицине гидрокарбонат натрия используется для нейтрализации кислотности желудочного сока и лечения изжоги.
- Сода также находит применение в промышленности, например, для пожаротушения, где гасят пламя путем выделения углекислого газа (CO2) и снижения температуры окружающей среды.
- В кулинарии гидрокарбонат натрия используется для приготовления теста, чтобы оно стало пышным и мягким.
- При хранении соды необходимо соблюдать безопасность и избегать контакта с кислотами или другими веществами, которые могут вызвать ее неконтролируемое распадание.
- Срок годности гидрокарбоната натрия начинает уменьшаться с момента вскрытия упаковки, поэтому рекомендуется использовать его в течение определенного периода времени.
- В кулинарии гидрокарбонат натрия также добавляют в кефир для получения идеального теста.
- Гидрокарбонат натрия имеет значительное значение в бытовом хозяйстве, где его используют для решения различных задач, например, для очистки поверхностей или удаления запахов.
Soda + уксус = ацетат натрия + углекислый газ + вода
Сочетание соды с уксусом представляет собой химическую реакцию, в результате которой образуется ацетат натрия, углекислый газ и вода. Эта реакция происходит при смешивании соды (гидрокарбоната натрия) с уксусом (уксусной кислотой). Свойства и применение этого соединения широко известны и находят применение в различных областях.
Свойства гидрокарбоната натрия
Гидрокарбонат натрия имеет белый кристаллический вид и является нерастворимым в спирте, но хорошо растворяется в воде. Он обладает щелочными свойствами и может нейтрализовать кислоты. Кроме того, гидрокарбонат натрия может распадаться при нагревании, выделяя углекислый газ и воду.
Применение гидрокарбоната натрия
Гидрокарбонат натрия находит широкое применение в различных областях, включая:
- Кулинария: в качестве разрыхлителя для теста, добавляют соду в сочетании с кефиром или уксусом, чтобы запустить химическую реакцию и получить углекислый газ, который заставляет тесто подниматься.
- Медицина: гидрокарбонат натрия используется в качестве средства для нейтрализации кислот, также он может помочь при изжоге и других желудочно-кишечных проблемах.
- Хозяйки используют соду для очистки и дезинфекции различных поверхностей.
- Промышленность: гидрокарбонат натрия используется в производстве стекла, моющих средств, керамики и других продуктов.
Важно учитывать, что при хранении гидрокарбоната натрия необходимо соблюдать определенные меры безопасности. Так, например, сода несовместима с кислотами и может вызвать реакцию с выделением угольной кислоты (углекислого газа) в виде пены. Поэтому не рекомендуется хранить соду вместе с кислотами.
Термическое разложение гидрокарбоната натрия происходит при температуре выше 50 градусов Цельсия. При нагревании сода начинает распадаться на ацетат натрия, углекислый газ и воду.
Идеальным сочетанием для гасения пожара с помощью соды является ее сочетание с уксусом. При смешивании соды с уксусом происходит реакция, в результате которой выделяется углекислый газ, который гасит огонь.
В химии гидрокарбонат натрия обозначается формулой NaHCO3. Ацетат натрия — это соль уксусной кислоты, обозначается формулой CH3COONa.
В заключение, сочетание соды с уксусом является химической реакцией, которая приводит к образованию ацетата натрия, углекислого газа и воды. Это сочетание находит применение в кулинарии, медицине, хозяйстве и промышленности. При хранении соды необходимо соблюдать меры безопасности, так как она может реагировать с кислотами и вызывать выделение углекислого газа.
Читайте далее: